
Предвосхищая вопросы некоторых читателей данного журнала о связи фармаконадзора с GDP, поясню, что связь действительно существует.
Фармаконадзор – вид деятельности, связанный с мониторингом эффективности и безопасности лекарственных препаратов, направленный на выявление, оценку и предотвращение нежелательных последствий применения лекарственных препаратов. Регулируется нормативно-правовым актом ЕАЭС – решением Совета Евразийской экономической комиссии от 3 ноября 2016 года № 87 «Об утверждении Правил надлежащей практики фармаконадзора».
Фармаконадзор в РФ осуществляется Росздравнадзором на основании сведений, полученных, в том числе, от субъектов обращения лекарственных средств (ЛС).
Дистрибьютор (организация оптовой торговли ЛС) относится к субъектам обращения ЛС и принимает участие в системе фармаконадзора.
После регистрации и начала производства лекарственный препарат попадает на рынок. Производители продолжают следить за ним, собирая данные о побочных действиях и нежелательных явлениях, не выявленных в процессе клинических испытаний. Накопленные сведения могут привести к изменениям в инструкции, отзыву препарата с рынка, прекращению производства или аннулированию государственной регистрации.
Самые достоверные данные получают от пациентов, медицинских и фармацевтических работников. Жалобы на побочные действия препаратов клиенты могут адресовать в аптечные учреждения. Ближайшее к производителям звено – дистрибьютор, с которым они заключают договор на поставку ЛС. Поэтому наряду с соглашением по качеству поставщики заключают с дистрибьюторами соглашения по обмену данными по фармакобезопасности (фармаконадзору).
Соглашение по обмену данными по фармакобезопасности (СОДБ)
Единой формы документа нет, каждый производитель составляет его на своё усмотрение. Как правило, СОДБ включает:
- глоссарий по фармаконадзору (расшифровка понятий нежелательной реакции, нежелательного явления, жалоб на качество продукции),
- назначение и функционирование уполномоченного лица по фармаконадзору,
- сбор, обработка, управление, контроль качества, получение недостающих данных индивидуальных сообщений о нежелательных реакциях,
- форма передачи сведений по фармаконадзору производителю, сроки сообщения информации,
- прохождение обучения сотрудников нормам фармаконадзора, документирование обучения,
- контактные данные сторон.
Документ обязывает дистрибьютора собирать и передавать производителям информацию о нежелательных реакциях и явлениях на применение ЛС в короткие сроки. Сотрудники, работающие с данными о безопасности продукции, обязаны проходить обучение по вопросам фармаконадзора.
В современной фармацевтической практике нередко встречаются случаи, когда производители лекарств стремятся максимально расширить перечень требований к дистрибьюторам. Особенно это касается обязательств по мониторингу информации, связанной с безопасностью препаратов.
Производители настаивают на включении в соглашение пунктов об обязательном отслеживании данных в различных источниках: социальных сетях, интернет-ресурсах, печатных СМИ, научных журналах и других информационных каналах. При этом они часто ссылаются на то, что такие требования утверждены штаб-квартирой компании и являются обязательными для исполнения.
Важно понимать, что подобные требования способны создать для дистрибьютора дополнительные риски. Хотя производители порой утверждают, что эти пункты носят формальный характер и вряд ли будут проверяться, практика показывает, что в определённый момент компания-производитель может потребовать подтверждения выполнения этих обязательств.
На мой профессиональный взгляд, мониторинг открытых источников, включая научные публикации, является прямой обязанностью производителя ЛС, а не организации, занимающейся оптовой торговлей. Это обусловлено следующими факторами: производитель обладает необходимой экспертизой и ресурсами для анализа такой информации, мониторинг безопасности препарата входит в прямые обязанности держателя регистрационного удостоверения, дистрибьютор не имеет достаточной квалификации для оценки научных данных.
Поэтому при согласовании договора настоятельно рекомендую проявлять принципиальность в данном вопросе и исключать подобные требования из документации. Это поможет избежать потенциальных конфликтов и необоснованных претензий в будущем.
Как всё устроено у нас
Ответственное за фармаконадзор лицо назначается приказом генерального директора (руководитель отдела сертификации). В приказе указан сотрудник, который его замещает. Обязанности ответственного лица по фармаконадзору (ОЛФН) перечислены в функциональном профиле – приложении к приказу.
В системе менеджмента качества есть стандартная операционная процедура (СОП) «Участие в процессе фармаконадзора», описывающая деятельность компании.
Специалисты отделов сертификации и претензий передают ОЛФН всю информацию о нежелательных явлениях и реакциях, которая поступает по телефону, на электронный адрес, через форму обращения пользователя по вопросам фармакобезопасности на сайте компании, через личный кабинет клиента. Ответственное лицо доводит информацию до сведения производителя в течение 24 часов. Информация, связанная с нежелательными явлениями и реакциями при применении лекарственных препаратов, предоставляется по рекомендуемому образцу (рисунок 1).
 |
 |
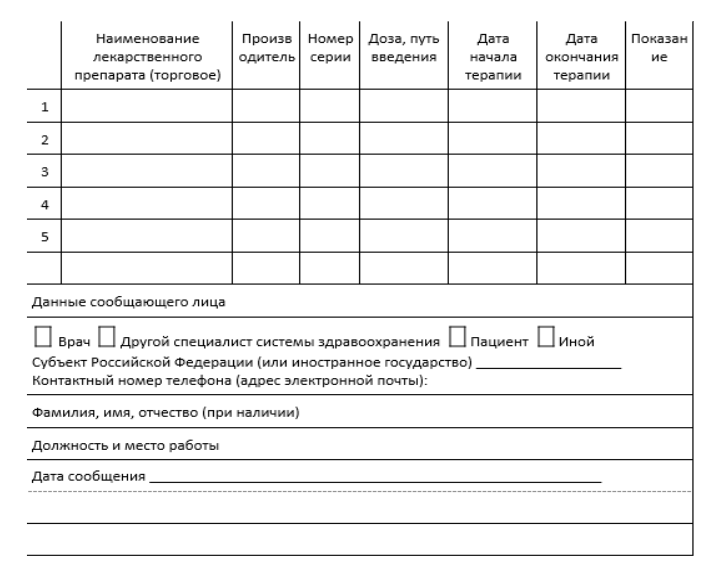 |
Рисунок 1.
Если характер сведений не соответствует содержанию бланка, допускается представление сведений в произвольной форме. При самостоятельном заполнении отчёта о нежелательном явлении (НЯ) или нежелательной реакции (НР), а также рекламации по качеству необходимо зафиксировать следующее: данные о пациенте, сведения о репортёре, описание события, информация о продукте, время ее получения.
Обучение по вопросам фармаконадзора
Обучение проходят сотрудники, работающие с информацией по безопасности продукции: ОЛФН, заместитель ОЛФН, руководитель отдела претензий, сотрудники отделов сертификации и претензий, секретари.
Ежегодно ОЛФН разрабатывает план обучения. Записи о проведенном обучении регистрируются в журнале. Оценка эффективности обучения проводится путём тестирования или собеседования с ОЛФН с фиксацией результатов в протоколе обучения.
Компании-производители регулярно проводят тренинги по фармаконадзору с тестированием и сообщают о нежелательных явлениях. Для сотрудников, получающих информацию о нежелательных реакциях (секретари, сотрудники ИТ), ОЛФН разрабатывает инструкцию.
История одного аудита
Наша компания-дистрибьютер проходила двухдневный аудит по фармаконадзору, который проводила специализированная иностранная компания-аудитор по поручению иностранного поставщика, поставляющего лекарственный препарат. Два дня, восемь часов, сотни вопросов, постоянные отсылки к подписанному соглашению по фармакобезопасности конвертировались в отчет с замечаниями на несколько листов.
Взгляд со стороны на нашу систему указал направление для улучшений
Нами был создан САРА-план, мы обновили версию нашей СОП по фармаконадзору, значительно ее дополнив, создали дополнительный электронный адрес и форму обращения пользователя по вопросам фармакобезопасности на сайте компании (рисунок 2), провели обучение всех сотрудников, которым может поступать информация о нежелательных реакциях на применение препаратов, не пропустили тестовое письмо и тестовый телефонный звонок, правильно обработали полученную информацию, передали ее производителю.
 В заключение отметим, что фармаконадзор – полезная и нужная система. Здоровье пациентов и их безопасность – приоритет для всех участников рынка. Производители, изучающие жалобы на качество и эффективность лекарств, заслуживают высокой оценки.
В заключение отметим, что фармаконадзор – полезная и нужная система. Здоровье пациентов и их безопасность – приоритет для всех участников рынка. Производители, изучающие жалобы на качество и эффективность лекарств, заслуживают высокой оценки.
Источник – Сборник GDP Review 6 — VII Конференции «Логистика лекарственных средств»

