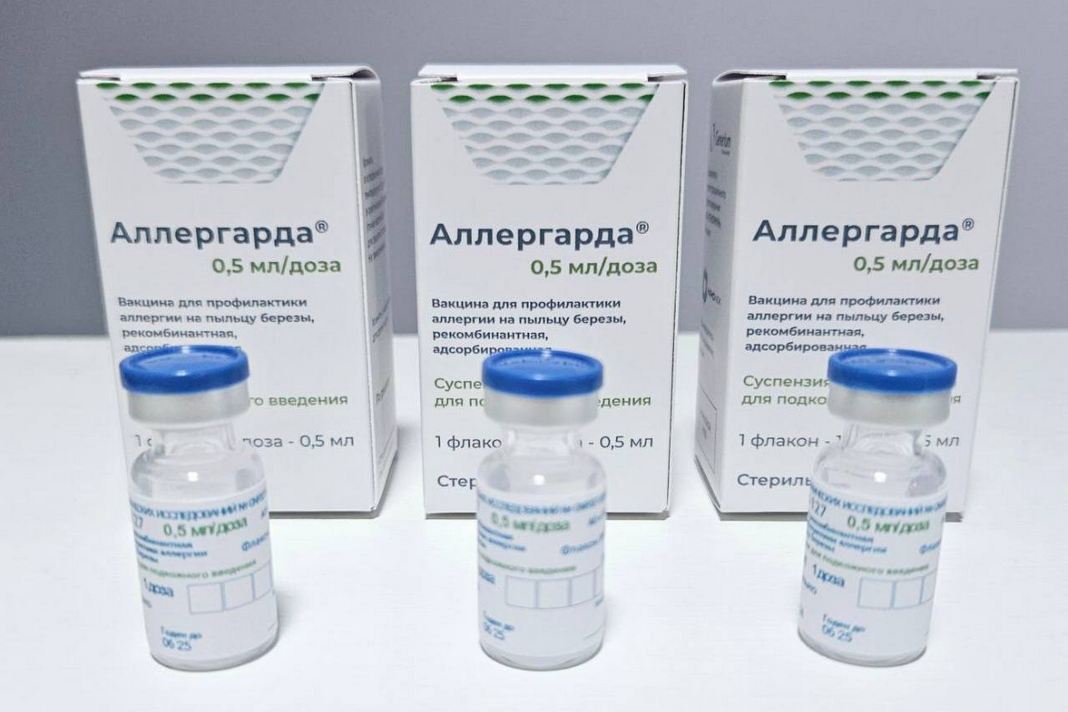
Федеральное медико-биологическое агентство (ФМБА) России официально подало документы на регистрацию уникальной рекомбинантной вакцины «Аллергарда», разработанной в ГНЦ «Институт иммунологии». Препарат предназначен для терапии аллергического ринита и перекрестной пищевой аллергии.
Ключевые факты:
- Продукт: Вакцина «Аллергарда» (рекомбинантная).
- Эффективность: Полное отсутствие симптомов у 25% пациентов; снижение интенсивности симптомов в 6 раз у остальных.
- Курс лечения: 3–5 инъекций (вместо 30 стандартных).
- Статус: Идет 3-я фаза КИ; выход в гражданский оборот ожидается во 2-й половине 2026 года.
Ход клинических исследований
В настоящий момент вакцина проходит третью фазу клинических исследований (КИ), в ходе которой её эффективность сравнивается с плацебо у пациентов с аллергическим ринитом. Результаты предыдущих этапов уже подтвердили высокий профиль безопасности и терапевтической активности препарата:
- У 25% добровольцев аллергические реакции исчезли полностью.
- У остальных участников группы интенсивность симптомов снизилась более чем в 6 раз.
- Серьезных нежелательных явлений в ходе испытаний зафиксировано не было.
Профиль препарата и преимущества
Ключевое отличие «Аллергарды» от классической аллерген-специфической иммунотерапии (АСИТ) — гипоаллергенность и кратно сокращенный курс лечения. Кроме того, вакцина обеспечивает защиту от перекрестной аллергии на продукты питания (яблоки, персики, арахис, соя).
| Параметр | Детали |
|---|---|
| Разработчик | ГНЦ «Институт иммунологии» ФМБА России |
| Тип препарата | Рекомбинантная вакцина |
| Показания | Поллиноз (береза), перекрестная пищевая аллергия |
| Курс лечения | 3–5 инъекций |
| Сравнение | Классические методы требуют ~30 инъекций |
| Срок выхода | II половина 2026 года (прогноз) |
Выход на рынок
Согласно прогнозам экспертов, процесс регистрации завершится в конце 2025 – начале 2026 года. При успешном окончании финальной фазы испытаний вакцина должна поступить в гражданский оборот во второй половине 2026 года.